科大领导团队研发机器学习模型CELLO2 揭示脑胶质瘤演化的预测因素
由香港科技大学(科大)领导的国际科研团队,近日揭示了原发性脑肿瘤在接受治疗时的恶化机制,并研究出一套人工智能模型,可预测脑癌患者接受治疗后的进程和结果,为改善病人管理策略以及实施精准肿瘤治疗提供新方向。
弥漫性脑胶质瘤是成年人最常见的原发性脑肿瘤,一般透过手术,并结合放射治疗与使用化学治疗药物-替莫唑胺(TMZ)进行治疗。然而,TMZ化疗往往只可延长患者约三个月的寿命,因为几乎所有患者都会面对脑胶质瘤复发的问题,而医学界至今仍未厘清这套标准疗法促使脑胶质瘤恶化的分子机制。
为解开这个谜团,由科大生命科学部和化学及生物工程学系夏利莱夫人生命科学副教授王吉光领导的研究团队,全面分析了544位脑胶质瘤患者的肿瘤分子样本和临床数据,当中包括182名东亚患者,以辨识不同种类脑胶质瘤演化的基因组和转录组预测因子。
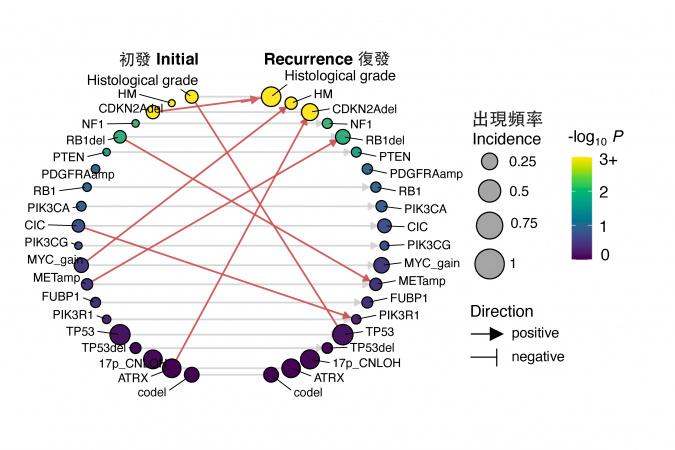
透过大数据分析,研究团队发现一些与TMZ抗药性及脑胶质瘤快速恶化相关的早期预测因子,包括患者于初次诊断时已发现调节基因MYC的数量增多,或MYC的目标基因被过度激发,这些情况均会诱发肿瘤在治疗时发生超突变。团队亦发现,如患者于初次诊断时,已发现CDKN2A基因缺失,他们后期肿瘤急剧恶化的机率亦更高。
团队亦进一步发现,东亚人的脑肿瘤基因突变,跟白人比较有明显差异。例如东亚患者脑肿瘤出现7号染色体扩增和10号染色体缺失的机率较少,而出现MYC 复制基因扩增的机率则相对较多。至于一种较常在白人患者身上发现的脑胶质瘤高风险因素rs55705857(G),却极少机会在东亚人群中出现。
王教授说:「这些研究结果印证了为癌症患者制定个人化治疗方案的重要性。我们相信发现这些脑胶质瘤复发的早期预测因子,将有助发展针对这种恶性肿瘤的精准治疗,尤其能为复发患者带来裨益。」
为了更好地评估患者接受治疗的进程及结果,研究团队开发了一套名为CELLO2的机器学习模型,用于初诊后评估患者的病情。经过训练的模型可以准确预测复发的肿瘤会否在TMZ化疗下恶化,并识别高风险患者。
为了让公众能够使用预测模型,团队特意设立一个公开的互动网站(CELLO2),为患者和医生提供脑胶质瘤的长期追踪数据库,并可根据患者的临床和基因组特征,预测TMZ化疗所诱发的肿瘤超突变和恶化的进程。这个平台对患者来说是一个重要的工具,让他们能够更深入地了解脑肿瘤的恶性程度。
首都医科大学北京天坛医院教授暨北京市神经外科研究所所长江涛教授表示:「胶质瘤患者往往面对复发,CELLO2是第一个可以通过原发肿瘤的分子特征预测复发肿瘤级别是否升高或耐药的有效工具,为临床管理患者和预估患者预后提供了重要参照。」
这项研究与北京天坛医院、韩国三星医学中心和香港中文大学(中大)韦尔斯亲王医院等合作完成。研究成果最近于《科学转化医学》期刊上发表。
未来,团队将透过整合更多患者数据,进一步优化机器学习模型,有助研究其他导致脑肿瘤产生抗药性的分子机制。团队现正与中大、北京天坛医院和上海华山医院合作,开发一个整合医学影像和多组学数据的人工智能平台,推动精准神经肿瘤学的发展。
(原文由香港科技大学环球事务及传讯处在此发布。)